Nukleofilní konjugovaná adice
Nukleofilní konjugovaná adice je druh organické reakce, zvláštní případ nukleofilní adice. Běžné nukleofilní adice probíhají většinou u karbonylových sloučenin. Jednodušší alkenové sloučeniny nevykazují 1,2-reaktivitu kvůli chybějící polaritě, pokud alkeny nejsou aktivovány zvláštními substituenty. U α,β-nenasycených karbonylových sloučenin jako je cyklohexenon lze z rezonančních struktur odvodit, že β pozice je elektrofilním místem, které může reagovat s nukleofilem. Záporný náboj je v těchto strukturách tvořen alkoxidovým aniontem. Taková nukleofilní adice se nazývá nukleofilní konjugovaná adice nebo 1,4-nukleofilní adice. Nejdůležitějšími aktivovanými alkenovými sloučeninami jsou výše zmíněné karbonylové sloučeniny a také akrylonitrily.
Reakční mechanismus
[editovat | editovat zdroj]Konjugovaná nukleofilní adice je vinylogním protějškem přímé nukleofilní adice. Nukleofil reaguje s α,β-nenasycenou karbonylovou sloučeninou na β pozici. Záporný náboj nukleofilu je nyní delokalizován v alkoxidovém aniontu a α uhlíkovém karboaniontu. Protonace probíhá přes keto-enol tautomerii k nasycené karbonylové sloučenině. Při vicinální difunkcionalizaci je proton nahrazen jiným elektrofilem.
Reakce
[editovat | editovat zdroj]- Konjugované karbonyly reagují se sekundárními aminy za vzniku 3-aminokarbonylových sloučenin (3-ketoaminů), například konjugovanou adicí methylaminu na cyklohexen-2-on vzniká 3-(N-methylamino)-cyklohexanon.
- Konjugované karbonyly reagují s kyanovodíkem za vzniku 1,4-ketonitrilů.
- Gilmanova činidla jsou účinnými nukleofily pro 1,4-adice na konjugované karbonyly
- Michaelova reakce zahrnuje adici enolátu na konjugované karbonylové sloučeniny.
- Storkova enaminová reakce zahrnuje adici enaminů na konjugované karbonylové sloučeniny.
Přehled
[editovat | editovat zdroj]Konjugovaná adice je užitečná pro tvorbu nových vazeb uhlík-uhlík za pomoci organokovových činidel, například reakcí organojodidů zinku s methylvinylketonem.
![(4R',5R')-5-(5-ethyl-2,2-dimethyl-[1,3]-dioxolan-4-yl)-pentan-2-on](http://upload.wikimedia.org/wikipedia/commons/7/7b/Conjugateadditionexample.png)
Příkladem asymetrické syntézy za použití konjugované nukleofilní adice je syntéza (R)-3-fenyl-cyklohexanonu z cyklohexenonu, kyseliny fenylborité a chirálního ligandu BINAP (katalyzátorem je acetylacetonát rhodia).

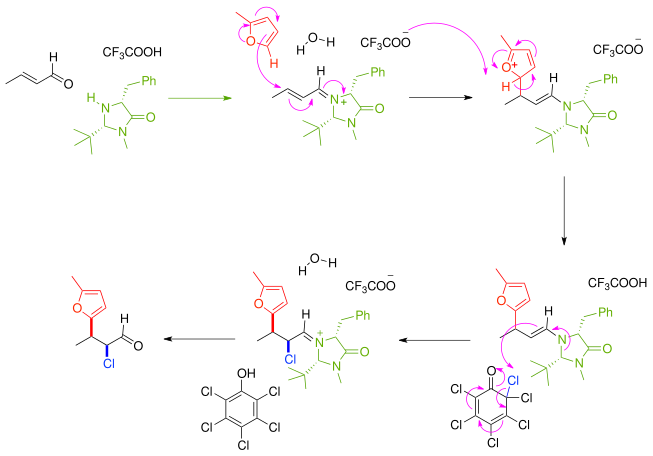
V dalším příkladu asymetrické syntézy nejprve α,β-nenasycená karbonylová sloučenina reaguje s chirálním imidazolidinonovým katalyzátorem a další chirální látkou za vzniku iminiové sloučeniny alkylimino-de-oxo-bisubstitucí; tato sloučenina následně enantioselektivně reaguje s furanovým nukleofilem, čímž se utvoří enamin, následuje kaskáda reakcí, při níž je odstraněn chlor z chlorovaného chinonu. Po odstranění aminového katalyzátoru je keton efektivně funkcionalizován.
Tento princip je také využíván při enantioselektivní vícesložkové dominové konjugované adici nukleofilních thiolů jako je benzylthiol na elektrofilní diethylazodikarboxylát.

Toxikologie
[editovat | editovat zdroj]Rozpustné Michaelovy akceptory jsou toxické, jelikož alkylují DNA konjugovanou adicí. Některé takto způsobené změny vyvolávají mutace, což má cytotoxické a karcinogenní účinky. S těmito látkami ovšem mohou rovněž reagovat glutathion a dimethylfumarát.
Reference
[editovat | editovat zdroj]V tomto článku byl použit překlad textu z článku Nucleophilic conjugate addition na anglické Wikipedii.
