Trifluormethansulfonát skanditý
Vzhled
| Trifluoromethansulfonát skanditý | |
|---|---|
 Strukturní vzorec | |
 Model krystalové struktury hydrátu | |
| Obecné | |
| Systematický název | trifluoromethansulfonát skanditý |
| Triviální název | triflát skanditý |
| Anglický název | Scandium(III) trifluoromethanesulfonate |
| Sumární vzorec | C3F9O9S3Sc |
| Identifikace | |
| Registrační číslo CAS | 144026-79-9 |
| PubChem | 2734571 |
| SMILES | C(F)(F)(F)S(=O)(=O)[O-].C(F)(F)(F)S(=O)(=O)[O-].C(F)(F)(F)S(=O)(=O)[O-].[Sc+3] |
| InChI | InChI=1S/3CHF3O3S.Sc/c3*2-1(3,4)8(5,6)7;/h3*(H,5,6,7);/q;;;+3/p-3 |
| Vlastnosti | |
| Molární hmotnost | 492,16 g/mol |
| Bezpečnost | |
| [1] Varování[1] | |
Některá data mohou pocházet z datové položky. | |
Trifluormethansulfonát skanditý, též triflát skanditý, je organická sloučenina, skanditá sůl kyseliny trifluormethansulfonové. Používá se jako reaktant v organické chemii, kde funguje jako Lewisova kyselina.[2] Na rozdíl od ostatních Lewisových kyselin je stabilní vůči vodě a v organických reakcích může být často použit jako skutečný katalyzátor místo použití ve stechiometrickém množství. Získává se reakcí oxidu skanditého a kyseliny trifluormethansulfonové.
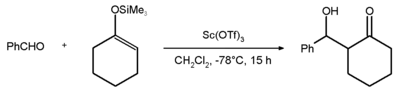
Příkladem použití této látky je Mukaijamova aldolová adice benzaldehydu se silylenoletherem cyklohexanonu (s výtěžností 81 %):
Reference
[editovat | editovat zdroj]V tomto článku byl použit překlad textu z článku Scandium(III) trifluoromethanesulfonate na anglické Wikipedii.
- ↑ a b Scandium(III) trifluoromethanesulfonate. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- ↑ Deborah Longbottom. SYNLETT Spotlight 12: Scandium Triflate. Synlett. 1999, s. 2023. DOI 10.1055/s-1999-5997.
Externí odkazy
[editovat | editovat zdroj] Obrázky, zvuky či videa k tématu Trifluormethansulfonát skanditý na Wikimedia Commons
Obrázky, zvuky či videa k tématu Trifluormethansulfonát skanditý na Wikimedia Commons