Cysteamin
| Cysteamin | |
|---|---|
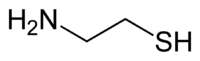 Strukturní vzorec | |
 Model molekuly | |
| Obecné | |
| Systematický název | 2-aminoethan-1-thiol |
| Sumární vzorec | C2H7NS |
| Vzhled | bílá pevná látka[1] |
| Identifikace | |
| Registrační číslo CAS | 60-23-1 |
| EC-no (EINECS/ELINCS/NLP) | 200-463-0 |
| PubChem | 6058 |
| ChEBI | 17141 |
| SMILES | C(CS)N |
| InChI | InChI=1S/C2H7NS/c3-1-2-4/h4H,1-3H2 |
| Vlastnosti | |
| Molární hmotnost | 77,149 g/mol |
| Teplota tání | 98 °C (371 K)[1] |
| Teplota varu | rozklad[1] |
| Rozpustnost ve vodě | rozpustný[1] |
| Rozpustnost v polárních rozpouštědlech | rozpustný v methanolu a ethanolu[1] |
| Bezpečnost | |
| [1] | |
| H-věty | H302 H315 H319 H335[1] |
| P-věty | P261 P264+265 P270 P271 P280 P301+317 P302+352 P304+340 P305+351+338 P319 P321 P330 P332+317 P337+317 P362+364 P403+233 P405 P501[1] |
Některá data mohou pocházet z datové položky. | |
Cysteamin (systematicky 2-aminoethanthiol) je organická sloučenina se vzorcem HSCH2CH2NH2, obsahující aminovou i thiolovou funkční skupinu. Často se používá v podobě solí, jako jsou hydrochlorid, fosfocysteamin, a hydrogenvinan.[2]
Tato látka vzniká (společně s kyselinou pantothenovou) rozkladem pantetheinu, který je sám produktem rozkladu koenzymu A.[2]
Slouží jako biosyntetický prekurzor neurotransmiteru hypotaurinu.[3]
Použití
[editovat | editovat zdroj]Cysteamin se používá na léčbu cystinózy, nemoci doprovázené nadměrným hromaděním cystinu, oxidovaného dimeru aminokyseliny cysteinu.[4] Pomáhá odstraňovat přebytečný cystin z buněk.[2] Lze jej přijímat ústně i v podobě očních kapek.[5][6][7][8]
Při povrchové aplikaci může tato látka zesvětlit kůži, která ztmavla v důsledku pozánětové hyperpigmentace, vystavení slunečnímu světlu, nebo melasmy.[9][10][11][12]
Povrchová aplikace cysteaminu se při léčbě melasmy ukázala být podobně účinnou jako intradermálně podaná kyselina tranexamová, ale měla výrazně méně vedlejších účinků.[13]
Vedlejší účinky
[editovat | editovat zdroj]Při povrchovém použití
[editovat | editovat zdroj]Cysteamin má méně vedlejších účinků než jiné podobně používané přípravky.[13]
Při ústním podání
[editovat | editovat zdroj]Ústně podávaný cysteamin může vyvolávat příznaky podobné Ehlersovu-Danlosovu syndromu, vyrážky na kůži, vředy a/nebo krvácení v žaludku a střevech a příznaky související s centrální nervovou soustavou, jako jsou záchvaty, ospalost, deprese, encefalopatie, snížení počtu bílých krvinek, zvýšenou úroveň alkalické fosfatázy, bolesti hlavy, a nevolnosti.[5]
Vliv cysteaminu na plod není znám, ale tato látka u zvířecích mláďat způsobuje poškození v nižších dávkách, než v jakých se podává lidem.[14][15]
U očních kapek jsou nejčastějšími vedlejšími účinky zvýšená citlivost na světlo, zarudnutí, bolesti hlavy, a poruchy vidění.[15]
Interakce
[editovat | editovat zdroj]V očních kapkách nebo běžných kapslích cysteamin nevykazuje žádné lékové interakce,[14][15] ale kapsle s prodlouženým uvolňováním by neměly být používány s léky ovlivňujícími tvorbu žaludeční kyseliny, jako jsou inhibitory protonové pumpy, nebo s alkoholem, které mohou způsobit příliš rychlé uvolnění léčiva.[5] Cysteamin neinhibuje žádný z enzymů cytochromu P450.[5]
Farmakologické vlastnosti
[editovat | editovat zdroj]U lidí s cystinózou není přítomen fungující přenašeč (cystinosin) převádějící cystin z lyzozomu do cytosolu, což vede ke hromadění cystinu v lyzozomech, kde krystalizuje a poškozuje buňky.[16]
Cysteamin proniká do lyzozomů a přeměňuje cystin na cystein a cystein-cysteamidisulfid, které mohou být z lyzozomů vyloučeny.[5]
Cysteamin také usnadňuje transport L-cysteinu do buněk.[2]
Odkazy
[editovat | editovat zdroj]Reference
[editovat | editovat zdroj]V tomto článku byl použit překlad textu z článku Cysteamine na anglické Wikipedii.
- ↑ a b c d e f g h https://pubchem.ncbi.nlm.nih.gov/compound/6058
- ↑ a b c d M. Besouw; R. Masereeuw; L. van den Heuvel; E. Levtchenko. Cysteamine: an old drug with new potential. Drug Discovery Today. 2013, s. 785–792. DOI 10.1016/j.drudis.2013.02.003. PMID 23416144.
- ↑ T. P. Singer. Metabolic pathways: Metabolism of sulfur compounds. [s.l.]: Academic Press, 1975. ISBN 9780323162081. Kapitola Oxidative Metabolism of Cysteine and Cystine, s. 545.
- ↑ W. A. Gahl; J. G. Thoene; J. A. Schneider. Cystinosis. The New England Journal of Medicine. 2002, s. 111-121. DOI 10.1056/NEJMra02055. PMID 12110740.
- ↑ a b c d e Procysbi- cysteamine bitartrate capsule, delayed release pellets Procysbi- cysteamine bitartrate granule, delayed release [online]. U.S. National Library of Medicine [cit. 2020-04-27]. Dostupné online.
- ↑ Procysbi EPAR [online]. [cit. 2020-04-27]. Dostupné online.
- ↑ Cystagon EPAR [online]. 2007-10-16 [cit. 2020-04-27]. Dostupné online.
- ↑ Cystadrops EPAR [online]. 2017-02-22 [cit. 2020-04-27]. Dostupné online.
- ↑ C. Hsu; H. Mahdi; M. Pourahmadi; S. Ahmadi. Cysteamine cream as a new skin depigmenting product. Journal of the American Academy of Dermatology. 2013, s. AB189. Dostupné online. DOI 10.1016/j.jaad.2012.12.781.
- ↑ Cysteamine cream [online]. [cit. 2021-06-29]. Dostupné online.
- ↑ P. E. Grimes; S. Ijaz; R. Nashawati; D. Kwak. New oral and topical approaches for the treatment of melasma. International Journal of Women's Dermatology. 2019, s. 30-36. DOI 10.1016/j.ijwd.2018.09.004. PMID 30809577.
- ↑ P. Mansouri; S. Farshi; Z. Hashemi; B. Kasraee. Evaluation of the efficacy of cysteamine 5% cream in the treatment of epidermal melasma: a randomized double-blind placebo-controlled trial. The British Journal of Dermatology. 2015, s. 209-217. DOI 10.1111/bjd.13424. PMID 25251767.
- ↑ a b L. Hilton. Cysteamine cream, tranexamic acid mesotherapy reveal similar efficacy, different safety [online]. 2020-10-14 [cit. 2021-06-29]. Dostupné online.
- ↑ a b Cystagon- cysteamine bitartrate capsule [online]. 2019-01-29 [cit. 2020-04-27]. Dostupné v archivu pořízeném z originálu dne 2021-03-25.
- ↑ a b c Cystaran- cysteamine hydrochloride solution [online]. 2019-11-22 [cit. 2020-04-27]. Dostupné online.
- ↑ G. Nesterova; W. A. Gahl. GeneReviews. [s.l.]: University of Washington, 2016-10-06. PMID 20301574. Kapitola Cystinosis.

