Buněčná biologie

Buněčná biologie (také cytologie; řecky kytos - buňka + lat. logos - věda) je obor biologie, který studuje strukturu, funkci a chování buněk. Všechny živé organismy se skládají z buněk.[1][2] Buňka je základní jednotkou života, která je zodpovědná za život a fungování organismů.[3] Buněčná biologie se zabývá studiem strukturních a funkčních jednotek buněk. Buněčná biologie zahrnuje jak prokaryotické, tak eukaryotické buňky a má mnoho dílčích témat, která mohou zahrnovat studium buněčného metabolismu, buněčné komunikace, buněčného cyklu, biochemie a složení buněk. Studium buněk se provádí pomocí několika mikroskopických technik, buněčných kultur a buněčné frakcionace. Tyto techniky umožnily a v současné době se používají k objevům a výzkumu týkajícího se fungování buněk, což v konečném důsledku umožňuje pochopit větší organismy. Znalost složek buněk a jejich fungování je zásadní pro všechny biologické vědy a zároveň je nezbytná pro výzkum v biomedicínských oborech, jako je výzkum nádorových onemonění a další nemoci. Výzkum v oblasti buněčné biologie je propojen s dalšími obory, jako je genetika, molekulární genetika, molekulární biologie, lékařská mikrobiologie, imunologie a cytochemie.
Dějiny
[editovat | editovat zdroj]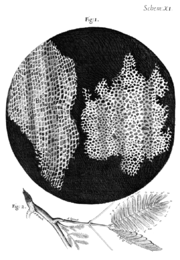
Obecné dějiny zkoumání buňky
[editovat | editovat zdroj]Buňky byly poprvé pozorovány v Evropě v 17. století s vynálezem složeného mikroskopu. V roce 1665 označil Robert Hooke stavební prvek všech živých organismů jako "buňky" poté, co si prohlédl kousek korku a pozoroval strukturu podobnou "klášterní cele mnichů" (lat. cella, tedy komora; latinské slovo pro buňku - cellula - pak znamená "malá cela").[4][5] Buňky však byly mrtvé a neposkytovaly žádné informace o skutečných celkových složkách buňky. O několik let později, v roce 1674, Antoni Van Leeuwenhoek jako první analyzoval živé buňky při zkoumání řas. Roku 1825 uveřejnil Jan Evangelista Purkyně první popis jádra živočišné buňky. S popisem jádra v rostlinné buňce jej následoval Robert Brown v roce 1831. To vše předcházelo vzniku buněčné teorie, která tvrdí, že vše živé se skládá z buněk a že buňky jsou funkční a strukturní jednotkou organismů. K tomuto závěru nakonec dospěli v roce 1838 rostlinný vědec Matthias Schleiden[5] a živočišný vědec Theodor Schwann, kteří si prohlédli živé buňky v rostlinné, respektive živočišné tkáni.[3] O 19 let později přispěl k teorii buňky Rudolf Virchow, který dodal, že všechny buňky vznikají dělením již existujících buněk.[3] Viry nejsou považovány za součást buněčné biologie - postrádají vlastnosti živé buňky a místo toho jsou studovány v mikrobiologické podtřídě virologie.[6]
Klinická cytologie
[editovat | editovat zdroj]Základy klinické cytologie položil v roce 1840 Johannes Müller, který rozpoznal a popsal nádorové bujení a dokázal rozlišit sarkom a karcinom.[7] Zhruba v téže době přednesli základní teze buněčné teorie Matthias Schleiden a Theodor Schwann, nezávisle na nich některé tyto zásady objevil a vyslovil i Purkyně. Během 19. a 20. století se prudce rozvíjela mikroskopie, jednak pokud jde o kvalitu, schopnosti a nové typy mikroskopů, jednak pokud jde o její druhou část zabývající se přípravou vzorku - tj. jeho fixací a barvením. Význam cytologie stoupal jak v biologických vědách, tak v medicíně, kde se cytologická vyšetření stala důležitou diagnostickou metodou v mnoha oblastech. Důležitý byl pro cytologii i prudký rozvoj úzce souvisejících vědních oborů, zejména biochemie, biofyziky a molekulární biologie, který umožnil více se zabývat chemickým složením buněk a chemickými procesy v nich.
Typy buněk a jejich struktura
[editovat | editovat zdroj]Existují dva základní typy buněk: prokaryotické a eukaryotické buňky. Prokaryotické buňky se od eukaryotických odlišují absencí buněčného jádra nebo jiné organely vázané na membránu.[8] Prokaryotické buňky jsou mnohem menší než buňky eukaryotické, což z nich činí nejmenší formu života.[9] Mezi prokaryotické buňky patří bakterie a archea a nemají uzavřené buněčné jádro. Eukaryotické buňky se vyskytují u rostlin, živočichů, hub a prvoků. Jejich průměr se pohybuje od 10 do 100 μm a jejich DNA je obsažena v membránou vázaném jádře.
Prokaryotická buňka
[editovat | editovat zdroj]
Bakterie mají několik různých tvarů, i když většina z nich má kulovitý nebo tyčinkovitý tvar. Bakterie lze podle složení buněčné stěny klasifikovat jako grampozitivní nebo gramnegativní. Grampozitivní bakterie mají silnější vrstvu peptidoglykanu než gramnegativní bakterie. Mezi strukturní znaky bakterií patří bičík, který pomáhá buňce v pohybu,[10] ribozomy pro překlad RNA na bílkoviny a nukleoid,[10] který v kruhové struktuře uchovává veškerý genetický materiál.[10] V prokaryotických buňkách probíhá mnoho procesů, které jim umožňují přežít. U prokaryot je syntéza mRNA zahájena na promotorové sekvenci na templátu DNA obsahující dvě konsenzuální sekvence, které rekrutují RNA polymerázu. Prokaryotická polymeráza se skládá z jádra enzymu složeného ze čtyř proteinových podjednotek a z proteinu σ, který pomáhá pouze při iniciaci. V procesu označovaném jako konjugace dochází k přenosu DNA na jinou bakterii, což umožňuje přenos rezistence umožňující přežití v určitých prostředích.[11]

Eukaryotická buňka
[editovat | editovat zdroj]Eukaryotické buňky se skládají z mnoha specializovaných organel:
- Jádro: Jádro buňky slouží jako úložiště genetické informace buňky (genom) a obsahuje veškerou DNA uspořádanou do podoby chromozomů. Je obklopeno jaderným obalem, který obsahuje jaderné póry umožňující transport proteinů mezi vnitřkem a vnějškem jádra.[12] Je to také místo replikace DNA a přepisu DNA do RNA. Poté je RNA upravena a transportována do cytosolu, kde je přeložena na bílkovinu.[13]
- Jadérko: Tato struktura se nachází uvnitř jádra, obvykle je hustá a má kulovitý tvar. Je místem syntézy ribozomální RNA (rRNA), která je potřebná pro sestavení ribozomů.
- Endoplazmatické retikulum (ER): Jeho funkcí je syntéza, skladování a vylučování bílkovin do Golgiho aparátu.[14] Strukturálně je endoplazmatické retikulum síť membrán, která se nachází v celé buňce a je spojena s jádrem. Membrány se v jednotlivých buňkách mírně liší a funkce buňky určuje velikost a strukturu ER.[15]
- Mitochondrie: obecně známá jako "elektrárna buňky" je buněčná organela vázaná na dvojitou membránu.[16] Slouží k výrobě energie neboli ATP v buňce. Konkrétně se jedná o místo, kde probíhá Krebsův cyklus pro výrobu NADH a FADH. Poté jsou tyto produkty použity v rámci elektronového transportního řetězce a oxidativní fosforylace pro konečnou výrobu ATP.[17]
- Golgiho aparát: Jeho funkcí je další zpracování, balení a vylučování proteinů na místo určení. Proteiny obsahují signální sekvenci, která umožňuje Golgimu aparátu jejich rozpoznání a nasměrovat na správné místo. Golgiho aparát také produkuje glykoproteiny a glykolipidy.[18]
- Lysozom: Lysozom slouží k rozkladu materiálu přineseného z vnějšku buňky nebo starých organel. Obsahuje mnoho kyselých hydroláz, proteáz, nukleáz a lipáz, které rozkládají různé molekuly. Autofagie je proces degradace prostřednictvím lysozomů, který probíhá tak, že se z ER oddělí váčky, která pohltí materiál a poté se připojí a spojí s lysozomem, aby umožnila degradaci materiálu.[19]
- Ribozomy: Slouží jako místo syntézy bílkovin.[20]
- Cytoskelet: Cytoskelet je struktura, která pomáhá udržovat tvar a celkovou organizaci cytoplazmy. Ukotvuje organely v buňkách a tvoří strukturu a stabilitu buňky. Cytoskelet se skládá ze tří hlavních typů proteinových filament: aktinová filamenta, intermediární filamenta a mikrotubuly, které jsou drženy pohromadě a spojeny se subcelulárními organelami a plazmatickou membránou pomocí různých pomocných proteinů.[21]
- Buněčná membrána: Buněčnou membránu lze popsat jako fosfolipidovou dvojvrstvu, která se rovněž skládá z lipidů a proteinů. Protože vnitřní strana dvojvrstvy je hydrofobní, a aby se molekuly mohly účastnit reakcí v buňce, musí být schopny tuto membránovou vrstvu překonat a dostat se do buňky prostřednictvím osmotického tlaku, difuze, koncentračních gradientů a membránových kanálů.[22]
- Centrioly: Vřeténková vlákna, která slouží k oddělování chromozomů při dělení buňky.
- Cilie: Některé buňky mohou být vybaveny i ciliemi, které mohou být použity i ke smyslovým účelům.[23]

Hlavní buněčné funkce
[editovat | editovat zdroj]Buněčný metabolismus
[editovat | editovat zdroj]Buněčný metabolismus je nezbytný pro produkci energie pro buňku, a tedy i pro její přežití, a zahrnuje mnoho dějů. Při buněčném dýchání probíhá v cytoplazmě buňky glykolýza, při níž z glukózy vzniká pyruvát. Pyruvát prochází dekarboxylací pomocí multienzymového komplexu za vzniku acetyl-CoA, který může být snadno využit v Krebsově cyklu k produkci NADH a FADH2. Tyto produkty jsou zapojeny do elektronového transportního řetězce, aby nakonec vytvořily protonový gradient přes vnitřní mitochondriální membránu. Tento gradient pak může pohánět produkci ATP během oxidativní fosforylace.[24] Metabolismus v rostlinných buňkách zahrnuje fotosyntézu, která je víceméně opakem dýchání, protože v konečném důsledku produkuje molekuly glukózy.
Buněčná signalizace
[editovat | editovat zdroj]Buněčná signalizace neboli buněčná komunikace je důležitá pro regulaci buněk a pro to, aby buňky zpracovávaly informace z okolí a odpovídajícím způsobem na ně reagovaly. K signalizaci může docházet prostřednictvím přímého kontaktu s buňkami nebo endokrinní, parakrinní a autokrinní signalizace. Přímý kontakt buňky s buňkou nastává, když receptor na buňce naváže molekulu, která je připojena k membráně jiné buňky. Endokrinní signalizace probíhá prostřednictvím molekul vylučovaných do krevního oběhu. Parakrinní signalizace využívá ke komunikaci molekuly difundující mezi dvěma buňkami. Autokrinní je buňka, která vysílá signál sama sobě vylučováním molekuly, která se váže na receptor na jejím povrchu. Formy komunikace mohou být prostřednictvím:
- Iontové kanály: Mohou být různých typů, například napěťově nebo ligandem řízené iontové kanály. Umožňují transport molekul a iontů.
- Receptor vázaný na G-protein (GPCR): Obsahují sedm transmembránových domén a na vnitrobuněčné straně membrány asociují s G-proteinem. Po navázání ligandu na extracelulární doménu dojde k produkci sekundárních poslů, jako je cAMP, IP3, DAG a vápník. Tito sekundární poslové fungují jako zesilovače signálů a mohou se vázat na iontové kanály nebo jiné enzymy.
- Tyrosinkinázové receptory: skupina receptorů, které se nachází na vnějším povrchu membrán buněk. Obsahují tyrosinkinázu, která přenáší fosfát na tyrosin. Mají vysokou afinitu k polypeptidům, jako jsou růstové faktory, cytokiny a některé hormony (především inzulin). Tyrosinkinasové receptory mají důležitou úlohu v rozvoji a vývoji mnoha typů rakoviny.[25]
Růst a vývoj buněk
[editovat | editovat zdroj]Buněčný cyklus eukaryotické buňky
[editovat | editovat zdroj]
Buňky jsou základem všech organismů a jsou základními jednotkami života. Růst a vývoj buněk je nezbytný pro udržení hostitele a přežití organismu. Při tomto procesu prochází buňka jednotlivými kroky buněčného cyklu a vývoje, které zahrnují růst buňky, replikaci DNA, dělení, regeneraci a smrt buňky.[26]
Buněčný cyklus je čtyřstupňový proces (fáze G1, S, G2 a M), kterým buňka prochází během svého vývoje a dělení. Fáze G - fáze růstu buňky - tvoří přibližně 95 % cyklu.[26] Proliferaci buněk iniciují progenitory. Všechny buňky začínají v identické podobě a mohou se stát v podstatě jakýmkoli typem buněk. Buněčná signalizace, například indukce, může ovlivnit blízké buňky a určit, jakým typem buňky se stanou. Navíc to umožňuje, aby se buňky stejného typu sdružovaly a vytvářely tkáně, poté orgány a nakonec systémy. Interfáze označuje fáze buněčného cyklu, které probíhají mezi jednou a druhou mitózou (zahrnují G1, S a G2), zatímco fáze M (mitóza) je částí cyklu, která se týká buněčného dělení. Mitóza se skládá z mnoha fází, které zahrnují profázi, metafázi, anafázi, telofázi a cytokinezi. Konečným výsledkem mitózy je vznik dvou identických dceřiných buněk. Buňka buď cyklus znovu zahájí od G1, nebo jej po dokončení cyklu opustí prostřednictvím G0.[26]
Buněčný cyklus je regulován v kontrolních bodech buněčného cyklu řadou signálních faktorů a komplexů, jako jsou cykliny, cyklin-dependentní kináza a p53. Když buňka dokončí svůj růstový proces a zjistí-li se, že je poškozená nebo změněná, podstoupí buněčnou smrt, a to buď apoptózou, nebo nekrózou, aby se eliminovala hrozba, kterou může způsobit přežití organismu.[27]
Kontrolní body buněčného cyklu a systém pro opravu DNA
[editovat | editovat zdroj]Buněčný cyklus se skládá z řady dobře uspořádaných, po sobě jdoucích fází, které vedou k buněčnému dělení. Buněčný cyklus je tedy sled činností, při nichž dochází k duplikaci buněčných organel a jejich následnému přesnému rozdělení na dceřiné buňky. Během buněčného cyklu dochází k několika hlavním událostem. Mezi procesy, které probíhají v buněčném cyklu, patří vývoj buňky, replikace a segregace chromozomů.[26]
Významným prvkem regulace buněčného cyklu je skutečnost, že buňky nezačínají další fázi, dokud není dokončena poslední.[28] Kontrolní body buněčného cyklu jsou dohledové systémy, které sledují integritu, přesnost a chronologii buněčného cyklu. Každý kontrolní bod slouží jako alternativní koncový bod buněčného cyklu, v němž se zkoumají parametry buňky, a teprve když jsou splněny žádoucí charakteristiky, postupuje buněčný cyklus jednotlivými kroky.[28]
Cílem buněčného cyklu je přesně zkopírovat DNA každého organismu a poté rovnoměrně rozdělit buňku a její součásti mezi dvě nové buňky. U eukaryot se vyskytují čtyři hlavní fáze. V G1 je buňka obvykle aktivní a pokračuje v rychlém růstu, zatímco v G2 pokračuje růst buňky, zatímco molekuly bílkovin se připravují na oddělení. Nejedná se o klidové období; v těchto fázích buňky nabírají hmotnost, integrují receptory růstových faktorů, vytvářejí replikovaný genom a připravují se na segregaci chromozomů.[26] Replikace DNA je u eukaryot omezena na samostatnou syntézu DNA, která je také známá jako S-fáze. Během mitózy, která je známá také jako fáze M, dochází k segregaci chromozomů.[29]
Dělení buněk je regulováno cyklin-dependentními kinázami, jejich přidruženými protějšky cykliny, proteinkinázami a fosfatázami, které regulují růst a dělení buněk od jedné fáze k druhé.[30] Buněčný cyklus je řízen časovou aktivací cyklin-dependentních kináz, která je řízena interakcí cyklinových partnerů, fosforylací konkrétními proteinkinázami a defosforylací fosfatázami rodiny Cdc25.
Smrtelnost buněk, nesmrtelnost buněčných linií
[editovat | editovat zdroj]Předci každé dnešní buňky pravděpodobně sahají v nepřerušené linii více než 3 miliardy let zpět ke vzniku života. Ve skutečnosti nejsou buňky nesmrtelné buňky, ale jsou to vícegenerační buněčné linie. Nesmrtelnost buněčné linie závisí na zachování potenciálu buněčného dělení.[31] Tento potenciál může být v každé konkrétní linii ztracen v důsledku poškození buňky, terminální diferenciace, k níž dochází u nervových buněk, nebo programované buněčné smrti (apoptózy) během vývoje. Udržení potenciálu buněčného dělení v následujících generacích závisí na zabránění a přesné opravě buněčných poškození, zejména poškození DNA.[31] U pohlavních organismů závisí kontinuita zárodečné linie na účinnosti procesů, které zabraňují poškození DNA a opravují poškození DNA, k nimž dojde. Pohlavní procesy u eukaryot, stejně jako u prokaryot, poskytují příležitost k účinné opravě poškození DNA v zárodečné linii pomocí homologní rekombinace.[32][33]
Autofagie
[editovat | editovat zdroj]Autofagie je autodegradační mechanismus, který reguluje zdroje energie během růstu a reakce na nutriční stres.[34] Autofagie také odstraňuje agregované proteiny a poškozené struktury včetně mitochondrií a endoplazmatického retikula a likviduje intracelulární infekce. Kromě toho má autofagie v buňce antivirovou a antibakteriální úlohu a podílí se na počátku rozlišovacích a adaptivních imunitních reakcí na virovou a bakteriální kontaminaci.[35] Některé viry obsahují proteiny virulence, které autofagii brání, zatímco jiné využívají prvky autofagie pro vnitrobuněčný vývoj nebo buněčné štěpení.[36]
Patologie a využití cytologie
[editovat | editovat zdroj]
Vědní obor, který studuje a diagnostikuje nemoci na buněčné úrovni, se nazývá cytopatologie. Na rozdíl od patologického oboru histopatologie, který zkoumá celé tkáně, se cytopatologie obvykle používá na vzorcích volných buněk nebo fragmentů tkání. Cytopatologie se běžně používá ke zkoumání onemocnění postihujících širokou škálu tělesných lokalit, často jako pomoc při diagnostice rakoviny, ale také při diagnostice některých infekčních onemocnění a jiných zánětlivých stavů. Běžnou aplikací cytopatologie je například Papův stěr, screeningový test používaný k odhalení rakoviny děložního čípku a přednádorových změn děložního čípku, které mohou vést ke karcinomu děložního hrdla.[37]
Dle zaměření se cytologie dělí na několik podoborů:
- cytopatologie (zkoumá změny na buňkách způsobené onemocněním či vnějšími vlivy)
- klinická cytologie (obor zabývající se cytologickými vyšetřeními pro potřeby lékařství), úzce souvisí s cytopatologií
- morfologická cytologie (zkoumá tvar a strukturu buněk)
- cytofyziologie (zabývá se mechanismy fungování buněk a jejich části)
- molekulární cytologie (v podstatě cytologická část molekulární biologie)
Metody a techniky buněčné biologie
[editovat | editovat zdroj]
Výzkum v oblasti buněčné biologie se zabývá různými způsoby kultivace a manipulace s buňkami mimo živé tělo za účelem dalšího výzkumu lidské anatomie a fyziologie a získávání léků. Techniky, kterými se buňky zkoumají, se neustále vyvíjejí a zdokonalují a umožňují tak vědcům neustále rozšiřovat znalosti nejenom na poli buněčné biologie. Díky pokroku v mikroskopii, technikám a technologiím umožnily vědcům lépe porozumět struktuře a funkci buněk. Níže je uvedeno mnoho technik běžně používaných ke studiu buněčné biologie:[38]
- Buněčné kultury: Využívá rychle rostoucí buňky na médiu, které umožňuje získat velké množství určitého typu buněk a představuje efektivní způsob studia buněk.[39] Buněčná kultura je jedním z hlavních nástrojů používaných v buněčné a molekulární biologii a poskytuje vynikající modelové systémy pro studium normální fyziologie a biochemie buněk (např. metabolické studie, stárnutí), účinků léčiv a toxických látek na buňky a mutageneze a karcinogeneze. Používá se také při screeningu a vývoji léčiv a při výrobě biologických sloučenin ve velkém měřítku (např. vakcín, terapeutických proteinů).
- Fluorescenční mikroskopie: Fluorescenční markery, jako je GFP, se používají k označení specifické složky buňky. Poté se k excitaci fluorescenčního markeru použije určitá vlnová délka světla, kterou lze následně vizualizovat.[39]
- Mikroskopie s fázovým kontrastem: Využívá optický aspekt světla k zobrazení změn v pevné, kapalné a plynné fázi jako rozdílu jasů.[39]
- Konfokální mikroskopie: Kombinuje fluorescenční mikroskopii se zobrazováním pomocí zaostřování světla a snímání případů, které vytvářejí trojrozměrný obraz.[39]
- Transmisní elektronová mikroskopie: Při této mikroskopii dochází k obarvení kovem a průchodu elektronů buňkami, které se při interakci s kovem vychýlí. Tím se nakonec vytvoří obraz studovaných složek.[39]
- Cytometrie: Buňky se umístí do přístroje, který je pomocí paprsku rozptýlí podle různých hledisek, a může je tak oddělit podle velikosti a obsahu. Buňky mohou být také označeny GFP-fluorescencí a mohou být separovány i tímto způsobem.[40]
- Frakcionace buněk: Tento proces vyžaduje rozbití buňky pomocí vysoké teploty nebo sonifikace a následnou centrifugaci, aby se oddělily jednotlivé části buňky a mohly být studovány odděleně.[39]
Významní buněční biologové
[editovat | editovat zdroj]- Jean Baptiste Carnoy
- Peter Agre
- Günter Blobel
- Robert Brown
- Geoffrey M. Cooper
- Christian de Duve
- Robert Hooke
- H. Robert Horvitz
- Marc Kirschner
- Anton van Leeuwenhoek
- Ira Mellman
- Peter D. Mitchell
- Rudolf Virchow
- Paul Nurse
- George Emil Palade
- Keith R. Porter
- Ray Rappaport
- Michael Swann
- Roger Tsien
- Edmund Beecher Wilson
- Kenneth R. Miller
- Matthias Jakob Schleiden
- Theodor Schwann
- Yoshinori Ohsumi
- Jan Evangelista Purkyně
Galerie
[editovat | editovat zdroj]-
Jan Evangelista Purkyně, objevitel Purkyňových buněk (1837)
-
Theodor Schwann, objevitel Schwannových buněk
-
Yoshinori Ohsumi, nositel Nobelovy ceny za objev autofagie
Související
[editovat | editovat zdroj]- Buňka
- Prokaryotická buňka
- Eukaryotická buňka
- Molekulární biologie
- Biochemie
- Organela
- Mikroskopie
- Mikrobiologie
Reference
[editovat | editovat zdroj]V tomto článku byl použit překlad textu z článku Cell biology na anglické Wikipedii.
- ↑ ALBERTS, Bruce; JOHNSON, Alexander D.; MORGAN, David; RAFF, Martin; ROBERTS, Keith; WALTER, Peter. Molecular Biology of the Cell. 6th. vyd. New York, NY: Garland Science, 2015. ISBN 978-0815344322. Kapitola Cells and genomes, s. 1–42.
- ↑ BISCEGLIA, Nick. Cell Biology [online]. www.nature.com. Dostupné online.
- ↑ a b c GUPTA, P. Cell and Molecular Biology. [s.l.]: Rastogi Publications, Dec 1, 2005. ISBN 978-8171338177. S. 11.
- ↑ HOOKE, Robert. Micrographia. [s.l.]: [s.n.], September 1665.
- ↑ a b CHUBB, Gilbert Charles. Encyclopædia Britannica. Příprava vydání Hugh Chisholm. 11. vyd. [s.l.]: Cambridge University Press 29 svazků. S. 710.
- ↑ Paez-Espino D, Eloe-Fadrosh EA, Pavlopoulos GA, Thomas AD, Huntemann M, Mikhailova N, Rubin E, Ivanova NN, Kyrpides NC. Uncovering Earth's virome. Nature. August 2016, s. 425–30. Dostupné online. DOI 10.1038/nature19094. PMID 27533034. S2CID 4466854. Bibcode 2016Natur.536..425P.
- ↑ MÜLLER, Johannes. On the Nature and Structural Characteristics of Cancer, and of Those Morbid Growths Which May Be Confounded with It. Med Chir Rev. 1840, s. 119–148. Dostupné online. PMID 29918423.
- ↑ DOBLE, Mukesh; GUMMADI, Sathyanarayana N. Biochemical Engineering. New Delhi: Prentice-Hall of India Pvt.Ltd, August 5, 2010. ISBN 978-8120330528.
- ↑ KANESHIRO, Edna. Cell Physiology Sourcebook: A Molecular Approach. 3rd. vyd. [s.l.]: Academic Press, May 2, 2001. ISBN 978-0123877383.
- ↑ a b c NELSON, Daniel. The Difference Between Eukaryotic And Prokaryotic Cells. Science Trends. 2018-06-22. DOI 10.31988/scitrends.20655. S2CID 91382191.
- ↑ GRIFFITHS, Anthony J.F.; MILLER, Jeffrey H.; SUZUKI, David T.; LEWONTIN, Richard C.; GELBART, William M. Bacterial conjugation. An Introduction to Genetic Analysis. 7th Edition. 2000. Dostupné online.
- ↑ DE ROOIJ, Johan. F1000Prime recommendation of Force Triggers YAP Nuclear Entry by Regulating Transport across Nuclear Pores..Chybí název periodika! 2019-06-25. DOI 10.3410/f.732079699.793561846. S2CID 198355737.
- ↑ Nucleus [online]. [cit. 2021-09-27]. Dostupné online. (anglicky)
- ↑ Endoplasmic Reticulum (Rough and Smooth) | British Society for Cell Biology [online]. [cit. 2019-10-06]. Dostupné online.
- ↑ STUDIOS, Andrew Rader. Biology4Kids.com: Cell Structure: Endoplasmic Reticulum [online]. [cit. 2021-09-27]. Dostupné online. (anglicky)
- ↑ Powerhouse of the cell has self-preservation mechanism [online]. [cit. 2021-09-27]. Dostupné online. (anglicky)
- ↑ PELLEY, John W. Elsevier's Integrated Biochemistry. [s.l.]: Elsevier, 2007. ISBN 9780323034104. DOI 10.1016/b978-0-323-03410-4.50013-4. Kapitola Citric Acid Cycle, Electron Transport Chain, and Oxidative Phosphorylation, s. 55–63.
- ↑ COOPER, Geoffrey M. The Golgi Apparatus. The Cell: A Molecular Approach. 2nd Edition. 2000. Dostupné online.
- ↑ VERITY, M A. Lysosomes: some pathologic implications.. [s.l.]: [s.n.] OCLC 679070471
- ↑ Ribosome | cytology [online]. [cit. 2021-09-27]. Dostupné online. (anglicky)
- ↑ The CELL A MOLEQULAR APPROACH. [s.l.]: Geoffrey M Cooper., 2000.
- ↑ COOPER, Geoffrey M. Transport of Small Molecules. The Cell: A Molecular Approach. 2nd Edition. 2000. Dostupné online.
- ↑ What Are the Main Functions of Cilia & Flagella? [online]. [cit. 2020-11-23]. Dostupné online. (anglicky)
- ↑ AHMAD, Maria; KAHWAJI, Chadi I. Biochemistry, Electron Transport Chain. StatPearls. StatPearls Publishing, 2019. Dostupné online [cit. 2019-10-20]. PMID 30252361.
- ↑ SCHLESSINGER, Joseph. Cell Signaling by Receptor Tyrosine Kinases. Cell. October 2000, s. 211–225. ISSN 0092-8674. DOI 10.1016/s0092-8674(00)00114-8. PMID 11057895. S2CID 11465988.
- ↑ a b c d e COOPER, Geoffrey M. The cell : a molecular approach. 2nd ed. vyd. Washington, D.C.: ASM Press xxiv, 689 pages s. Dostupné online. ISBN 0-87893-119-8, ISBN 978-0-87893-119-4. OCLC 43708665
- ↑ SHACKELFORD, R E; KAUFMANN, W K; PAULES, R S. Cell cycle control, checkpoint mechanisms, and genotoxic stress.. Environmental Health Perspectives. February 1999, s. 5–24. ISSN 0091-6765. DOI 10.1289/ehp.99107s15. PMID 10229703.
- ↑ a b ELLEDGE, Stephen J. Cell Cycle Checkpoints: Preventing an Identity Crisis. Science. 1996-12-06, roč. 274, čís. 5293, s. 1664–1672. Dostupné online [cit. 2023-02-21]. ISSN 0036-8075. DOI 10.1126/science.274.5293.1664. (anglicky)
- ↑ GIACOMELLO, Marta; PYAKUREL, Aswin; GLYTSOU, Christina; SCORRANO, Luca. The cell biology of mitochondrial membrane dynamics. Nature Reviews Molecular Cell Biology. 2020-02-18, s. 204–224. Dostupné online. ISSN 1471-0072. DOI 10.1038/s41580-020-0210-7. PMID 32071438. S2CID 211170966.
- ↑ NURSE, Paul. A Long Twentieth Century of the Cell Cycle and Beyond. Cell. 2000-01-07, s. 71–78. Dostupné online. ISSN 0092-8674. DOI 10.1016/S0092-8674(00)81684-0. PMID 10647932. S2CID 16366539. (English)
- ↑ a b IRFAN MAQSOOD, Muhammad; MATIN, Maryam M.; BAHRAMI, Ahmad Reza. Immortality of cell lines: challenges and advantages of establishment: Immortality of cell lines. Cell Biology International. 2013-10, roč. 37, čís. 10, s. 1038–1045. Dostupné online [cit. 2023-02-21]. DOI 10.1002/cbin.10137. (anglicky)
- ↑ Bernstein C, Bernstein H, Payne C. Cell immortality: maintenance of cell division potential. Prog Mol Subcell Biol. 2000;24:23-50. DOI:10.1007/978-3-662-06227-2_2. PMID 10547857.
- ↑ Avise JC. Perspective: The evolutionary biology of aging, sexual reproduction, and DNA repair. Evolution. 1993 Oct;47(5):1293-1301. DOI:10.1111/j.1558-5646.1993.tb02155.x. PMID 28564887.
- ↑ KLIONSKY, Daniel J. Autophagy revisited: a conversation with Christian de Duve. Autophagy. 2008-08, roč. 4, čís. 6, s. 740–743. PMID: 18567941. Dostupné online [cit. 2023-02-21]. ISSN 1554-8635. DOI 10.4161/auto.6398. PMID 18567941.
- ↑ MIZUSHIMA, Noboru; KOMATSU, Masaaki. Autophagy: renovation of cells and tissues. Cell. 2011-11-11, roč. 147, čís. 4, s. 728–741. PMID: 22078875. Dostupné online [cit. 2023-02-21]. ISSN 1097-4172. DOI 10.1016/j.cell.2011.10.026. PMID 22078875.
- ↑ GLICK, Danielle; BARTH, Sandra; MACLEOD, Kay F. Autophagy: cellular and molecular mechanisms. The Journal of Pathology. 2010-02-03, s. 3–12. Dostupné online. ISSN 0022-3417. DOI 10.1002/path.2697. PMID 20225336.
- ↑ What is Pathology? [online]. 2010-05-13 [cit. 2021-09-21]. Dostupné online. (anglicky)
- ↑ LAVANYA, P. Cell and Molecular Biology. [s.l.]: Rastogi Publications, Dec 1, 2005. ISBN 978-8171338177. S. 11.
- ↑ a b c d e f COOPER, Geoffrey M. Tools of Cell Biology. The Cell: A Molecular Approach. 2nd Edition. 2000. Dostupné online.
- ↑ MCKINNON, Katherine M. Flow Cytometry: An Overview. Current Protocols in Immunology. 2018-02-21, s. 5.1.1–5.1.11. ISSN 1934-3671. DOI 10.1002/cpim.40. PMID 29512141.
Externí odkazy
[editovat | editovat zdroj] Obrázky, zvuky či videa k tématu buněčná biologie na Wikimedia Commons
Obrázky, zvuky či videa k tématu buněčná biologie na Wikimedia Commons  Slovníkové heslo Buněčná biologie ve Wikislovníku
Slovníkové heslo Buněčná biologie ve Wikislovníku- Cytology and Genetics



