Arrheniova rovnice
Ve fyzikální chemii je Arrheniova rovnice rovnicí pro výpočet teplotní závislosti reakčních rychlostí. Rovnici představil Svante Arrhenius v roce 1889 na základě práce nizozemského chemika Jacobuse Henricus van 't Hoffa, který v roce 1884 poznamenal, že van 't Hoffova rovnice pro teplotní závislost rovnovážných konstant navrhuje takový vzorec pro rychlosti dopředné i zpětné reakce. Tato rovnice má rozsáhlé a důležité použití při určování rychlosti chemických reakcí a pro výpočet aktivační energie. Arrhenius poskytl fyzikální zdůvodnění a výklad pro vzorec.[1][2][3][4] V současné době je nanejvýš brána jen jako empirický vztah.[5] :s.188 Rovnice může být použita k modelování teplotních změn difúzních koeficientů, četnost krystalových vakancí, rychlosti tečení a mnoha dalších tepelně indukovaných procesů/reakcí. Eyringova rovnice, představená v roce 1935, také vyjadřuje vztah mezi rychlostí a energií.
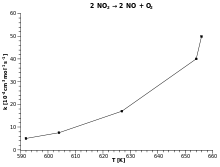
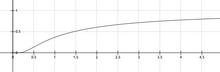
Arrheniova rovnice udává závislost rychlostní konstanty chemické reakce na absolutní teplotě jako:
Reference
[editovat | editovat zdroj]V tomto článku byl použit překlad textu z článku Arrhenius equation na anglické Wikipedii.
- ↑ ARRHENIUS, Svante. Über die Dissociationswärme und den Einfluss der Temperatur auf den Dissociationsgrad der Elektrolyte. zenodo.org. 1889-01-01. Dostupné online [cit. 2025-01-03]. DOI 10.1515/zpch-1889-0408.
- ↑ ARRHENIUS, Svante. Über die Reaktionsgeschwindigkeit bei der Inversion von Rohrzucker durch Säuren. zenodo.org. 1889-01-01. Dostupné online [cit. 2025-01-03]. DOI 10.1515/zpch-1889-0116.
- ↑ LAIDLER, Keith J. The development of the Arrhenius equation. Journal of Chemical Education. 1984-06-01, roč. 61, čís. 6, s. 494. Dostupné online [cit. 2025-01-03]. ISSN 0021-9584. DOI 10.1021/ed061p494.
- ↑ Laidler, K. J. (1987) Chemical Kinetics, Third Edition, Harper & Row, p. 42
- ↑ Kenneth Connors, Chemical Kinetics, 1990, VCH Publishers Chemical Kinetics: The Study of Reaction Rates in Solution na Knihách Google
Externí odkazy
[editovat | editovat zdroj] Obrázky, zvuky či videa k tématu Arrheniova rovnice na Wikimedia Commons
Obrázky, zvuky či videa k tématu Arrheniova rovnice na Wikimedia Commons



