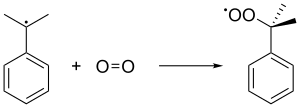Kumenový proces


Kumenový proces (Hockův proces) je chemický proces výroby fenolu a acetonu z benzenu a propenu; pojmenován je podle kumenu (isopropylbenzenu), vznikajícího jako meziprodukt. Objevili jej nezávisle na sobě R. Ūdris a P. Sergejev v roce 1942[1] a Heinrich Hock v roce 1944.[2][3]
Kromě benzenu a propenu slouží jako reaktanty vzdušný kyslík a malé množství radikálového iniciátoru.
Kroky
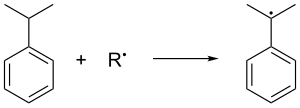
[editovat | editovat zdroj]Kumen se vyrábí Friedelovou–Craftsovou alkylací benzenu propenem. Směs benzenu a propenu se při teplotě 250 °C stlačuje na tlak 3 MPa za přítomnosti Lewisovy kyseliny (kyseliny fosforečné nebo hlinitého halogenidu) jako katalyzátoru. Vzniklý kumen se oxiduje na vzduchu, přičemž se z něj odštěpí terciární benzylový vodík a vytvoří se kumenový radikál:
Kumenový radikál se následně navazuje na kyslík za tvorby kumenperoxidového radikálu, z něhož se odštěpením benzylového vodíku z další molekuly kumenu stává kumenhydroperoxid (C6H5C(CH3)2O2H). Tlak 0,5 MPa udržuje nestálý peroxid v kapalném skupenství.
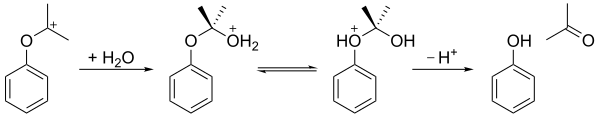
Kumenhydroperoxid se v kyselém prostředí přesmykuje (tato reakce se nazývá Hockův přesmyk) za vzniku fenolu a acetonu. Nejprve je protonován koncový kyslík hydrogenperoxidu. Následně se fenylová skupina přesouvá z benzylového uhlíku na sousední kyslík a odděluje se molekula vody, čímž vznikne rezonančně stabilizovaný terciární karbokation; soustředěný mechanismus této části je podobný jako mechanismus Baeyerovy–Villigerovy oxidace[4] a Criegeeova přesmyku a také oxidačnímu kroku hydroboračně–oxidačních reakcí.[5]
Tento karbokation poté reaguje s vodou a vytváří se poloacetal. Po přesunu protonu z hydroxylového kyslíku na etherový se ion rozpadne na fenol a aceton.
Podobné reakce
[editovat | editovat zdroj]Bez tvorby acetonu
[editovat | editovat zdroj]Kumen lze nahradit cyklohexylbenzenem. Cyklohexylbenzenhydroperoxid skrz Hockův přesmyk odštěpuje H+ za vzniku fenolu a cyklohexanonu; cyklohexanon poté lze použít na výrobu polyamidů.[6]
Při alkylaci benzenu směsí but-1-enu a but-2-enu jsou výsledky reakce fenol a butanon.[3]
Bez tvorby fenolu
[editovat | editovat zdroj]- Hydrochinon se vyrábí dialkylací benzenu propenem na 1,4-diisopropylbenzen, který pak reakcí se vzduchem vytváří bis(hydroperoxid).Podobně jako z kumenhydroperoxidu se pak tento meziprodukt přesmykuje, přičemž zde jsou produkty aceton a hydrochinon. Oxidací hydrochinonu lze získat 1,4-benzochinon:[7]
- 2 C6H4(CHMe2)2 + 5 O2 → 2 C6H4O2 + 4 OCMe2 + 2 H2O
- Obdobně se vyrábí resorcinol přeměnou 1,3-diisopropylbenzenu na bis(hydroperoxid), následně se štěpící na resorcinol a aceton.[8]
- 2-naftol lze také získat postupem analogickým ke kumenovému procesu.[9]
- 3-chlorfenol, který nelze vytvořit chlorací fenolu, může být získán obdobou kumenového procesu, kde se začíná alkylací chlorbenzenu propenem.[10]
- Krezoly se vyrábějí z isopropyltoluenů.[11]
Zpracování acetonu
[editovat | editovat zdroj]Surový aceton se často hydrogenuje za katalýzy Raneyovým niklem nebo oxidem měďnatého-chromitým na izopropylalkohol.[12]
Dehydratací izopropylalkoholu lze následně získat propen, znovu použitelný jako reaktant.[3]
Vedlejší produkty
[editovat | editovat zdroj]Vedlejšími produkty výroby fenolu a acetonu kumenovým procesem jsou acetofenon a alfa-methylstyren.
Odkazy
[editovat | editovat zdroj]Reference
[editovat | editovat zdroj]V tomto článku byl použit překlad textu z článku Cumene process na anglické Wikipedii.
- ↑ [cit. 2011-02-27]. Dostupné v archivu pořízeném z originálu dne 2016-03-03.
- ↑ Hock, H. and Lang, S. (1944), Autoxydation von Kohlenwasserstoffen, IX. Mitteil.: Über Peroxyde von Benzol-Derivaten. Berichte der deutschen chemischen Gesellschaft, 77: 257–264 DOI:10.1002/cber.19440770321
- ↑ a b c Jeffrey S. Plotkin. Direct Routes to Phenol [online]. [cit. 2006-12-26]. Dostupné v archivu pořízeném z originálu dne 2007-04-09.
- ↑ A. Streitwieser; C. H. Heathcock; E. M. Kosower. Introduction to Organic Chemistry. [s.l.]: [s.n.], 1992. ISBN 0-02-418170-6. Kapitola 30.
- ↑ K. P. C. Vollhardt; N. E. Schore. Organic Chemistry: Structure and Function. [s.l.]: [s.n.], 2003. ISBN 0-7167-4374-4. Kapitola 22.
- ↑ Jeffrey S. Plotkin. What's New in Phenol Production? [online]. American Chemical Society, 2016-03-21 [cit. 2018-01-02]. Dostupné v archivu pořízeném z originálu dne 2019-10-27.
- ↑ Gerhard Franz, Roger A. Sheldon "Oxidation" Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2000 DOI:10.1002/14356007.a18_261
- ↑ Ullmann's Encyclopedia of Industrial Chemistry. Příprava vydání Wiley-VCH. 1. vyd. [s.l.]: Wiley Dostupné online. ISBN 978-3-527-30385-4, ISBN 978-3-527-30673-2. DOI 10.1002/14356007.a23_111.pub2. (anglicky) DOI: 10.1002/14356007.
- ↑ Gerald Booth "Naphthalene Derivatives" Ullmann's Encyclopedia of Industrial Chemistry, 2005, Wiley-VCH, Weinheim DOI:10.1002/14356007.a17_009
- ↑ MULLER, François; CAILLARD, Liliane. Chlorophenols. Příprava vydání Wiley-VCH Verlag GmbH & Co. KGaA. Weinheim, Germany: Wiley-VCH Verlag GmbH & Co. KGaA Dostupné online. ISBN 978-3-527-30673-2. DOI 10.1002/14356007.a07_001.pub2. (anglicky) DOI: 10.1002/14356007.a07_001.pub2.
- ↑ Roger A. Sheldon. Syntheses and Uses of Hydroperoxides and Dialkylperoxides. [s.l.]: [s.n.], 1983. DOI 10.1002/9780470771730.ch6.
- ↑ Ullmann's Encyclopedia of Industrial Chemistry. Příprava vydání Wiley-VCH. 1. vyd. [s.l.]: Wiley Dostupné online. ISBN 978-3-527-30385-4, ISBN 978-3-527-30673-2. DOI 10.1002/14356007.a22_173.pub3. (anglicky) DOI: 10.1002/14356007.